你读完我们的本篇,应该会冒出冷汗:去听一个没有专业素养的人讲“手术后切口疼痛不是AE”这类笑话的免费让自己更加廉价,而有些同事早已经跳槽去外企CRA,就明白选择什么内容也是需要智商才能辨别真伪的,欢迎加入会籍。
为什么说CRA升迁PM的临界点,在于深刻理解“把site管得很好”?能把Site管得很好,说明他不是一个使蛮劲的,懂得每月每周每个site遇到的事情是有轻重缓急的、他们的受试者安排的随访很合理,你的effort在当下可以看到未来六个月将如何被消耗,你做出一个合理的估计,并且开始准备做一些草稿的内容,以避免将工作推到一起,搞到焦头烂额,这意味着你对目前的文档工作有一个合理的认识,清楚哪些docs是如何编码、启动前如何准备、实施中应如何管理。
例如,你的ICF,在签署时,应当单独拿出一个文件夹,每个受试者签署ICF,都集中存在里面,用铅笔在每个ICF上写筛选号、入组号,这样有助于管理。因为,按照要求,每次visit必须100%核查每个受试者的ICF,如果有修订、增补、撤除知情同意,都需要对这些变化的部分确认是否存在增加。当然,如今经过我们的培训,行业已经不会再犯错误“受试者撤除知情同意就是把ICF退回来”而是知道在ICF和病史中分别标记退出日期、原因和简要说明。
一个CRA,能把site管好,其实总为总监的上级,看一眼就非常清楚这个孩子行不行。他如果行,首先是自己能干,其次是他在工作过程遇到问题、觉得不对,不会不懂装懂,会找同事问、找领导请教,而且非常聪明的改善。
比如,你同时管理四个global试验,其中一个IV期处于随访中你需要管理860例受试者、三家中心;一个是关键II期,但是用于直接注册申报,每个case都不能出错误,两家中心都是非常专业的,入组量也在top级,做病理切片和影像学检查;还有两家site入组结束的全球III期,要做心血管事件随访,但SAE非常多;另外三家,要入组三期,但每个亚组都需要入一个block,而且要做BA、PK样本分析。
你可能注意到了,这四个试验、9家site,是我观察、分析和迅速剖析特点,开始制定我的工作计划。
我的监查计划,并不同于PM给的《Site Monitoring Plan》,我需要在在这个计划中,插入9个site的workload estimation,预期几个site如何启动、入组效率,以合理安排工作量分配。
更重要的,是我对自己的思考:我是将这家CRO当做跳板,尽快去另一家公司,还是希望在这家公司常驻?我是外企CRO跳外企药厂,那就是外企药厂之后只去外企药厂,我可能凭借外企CRO多领域经验拿到一个综合品种的外企Pharma机会,但我不喜欢这家企业什么项目都做,所以,我再过两年需要去某家外企,这意味着对公司不同的管线品种项目做出深刻理解,并分析出影响你晋升这些有一些深入的探讨,这个过程我们会有一些很好的附件,CRA在两百三十八篇课程中已经学到了,自己去找并下载即可。
比如说你的目标是大于这家公司工作?还是说你要跳槽去另外另一个目标城市?他们希望你有什么经验,你公司现在有没有?比如说恒瑞肿瘤的团队生得最快,那血管就没有价值吗? 你想做食管癌都会被挑剔因为目前biotech甚至要求必须做胃癌的经验、哪怕食道癌经验都不考虑,然后你要做减肥药呢等等?
所以很多事情并不是绝对的,很多机会,是在我们不断地深入思考中,动态变化、寻求和成长出来的,社会在变,我们也在变,风险和机会也在变,SWOT经典策略,我们的会员一直在用,详见我们视频号。
所以风险分析的运用其实很简单:外部、内部分线是什么?你去了巨头,一定能做到你喜欢的产品线吗?你一定会被重用吗?你和上级合拍吗?……
全球十余年来已成熟应用Risk Based Monitoring,在一线CRA实践中,产生很多相关技巧和方法,尤其是最主要角色CRA在其中应担当的思考和工作策略,部分外企实际上在中国已成熟运用。
在其它相关章节中,我们介绍Partial SDV、并介绍国外一些研究中SDV价值探讨,反映为何FDA和EMA为主的ICH区域,对非关键数据和流程数据的态度。
我们也介绍了国外外包服务提供商ESP监管走过的五个阶段,这些技术手段和目前Remote Monitoring, Centralized Monitoring,Risk Monitoring 理念应用是同步的。Monitoring的理解,可能很多同行理解存在不对的地方,并不是只有Moniotor去执行Monitoring的,还要有医学监查员,统计师,数据管理员,并介绍相关中枢化管理幻灯。
我们ctbmi属于专业运营、付费运作,如未连贯阅读,很难看懂。您加入会籍后,可整体、系统、连贯学习,欢迎加入会籍。
本篇课程,介绍的Adaptive Monitoring这一部分,也就是基于风险的监查理念。将以极其简练的方式,介绍风险管理工具在MonitoringPlan/Guidance中的应用,本文所提及的工具,内容包含外资企业对于Risk评估的具体表格,极具行业借鉴意义。考虑到MDRA和FDA都有Risk评估和管理工具,考虑范围较广,制药企业除非认识到风险管理的意义,否则没有任何应用价值。
这些表格模板,均是国外在2013年由某外企开发,并得到推广认可,在全球很多地区广泛使用。目前,基于这套工具,全球其他协会衍生出四个主要的变种标准,适应于不同的外企+CRO圈。用户可自行去互联网搜索这些内容。
简单的介绍下,如同我上述提及,ESP监管走过五个阶段,从最开始的低价中标,走到临床试验绩效矩阵合作(远不止于固定外包合作服务提供商那样简单)的第五阶段,基于风险管理分配关键资源到关键数据和流程环节,是申办方和ESP共同落实的措施,步骤,理念植入实践的根源。
普及一下相关风险管理的灵感和思路:

……略,CRA会员登录网站可见
为便于读者理解,我仅列举适用于B类的几种情况,

发现问题,重在找出问题的原因,并分析缓解措施的成本和得力植入结果,培训,和解决潜在问题,并作出有效的行动。
现场监查基于远程监查和中枢化分析,更有针对性,如下图所示
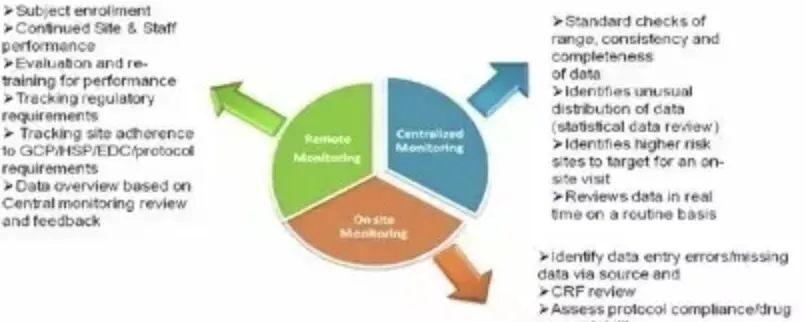
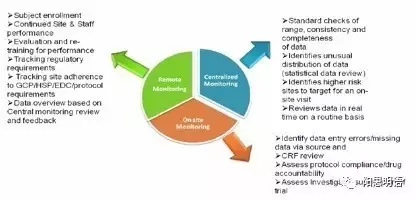

药政当局认为,申办方和监查员责任引起的问题,主要如下:
-监查措施不令人满意。需要注意的是,并不是一月一次固定监查,就意味着令人满意,监查的质量,效率,关键资源分配,问题预防和处理的程度,是更令人看重的指标
-不能确认研究者依从性。中国CRA自身素质客观上来说,长期缺乏企业系统性培训,所学知识极为有限,态度,社交礼仪更存在问题,医生主任属于全人类精英,这种对话过程和效果,可想而知。甚至大部分CRA,自身素质不佳,方案不熟,法规不精通,连和主任对话的基本素质都不具备,谈不上通过对话和行为观察其对方案的理解情况,和可能暴露的问题。(应该说,大部分CRA看不懂我这段话的意思吧?看懂的,都算是受过良好教育的)
-不能递交进度报告。中国在这一两年,开始学会年度报告和伦理定期审核的意义,虽然说象征性成分还是大了一些,但总归是进步。研究者可能连报告都没有时间去读,更不要提应由其起草,部分CRO在完成这些内容方面,更是存在缺失。这和国外完全由PI主动进行的情况,存在显著差别。
-药物……略,会员登录网站可见
……略,会员登录网站可见
CRA会员登录网站可见:【中心监查】系列三十三||为什么说“把site管得很好的CRA”,都擅长使用研究中心风险管理工具,并整合到《监查计划》中?
输入“会籍”查看模块,输入“付费”支付费用加入会籍。