独立工作的能力,不是独自工作,是独立的履行工作职责,明白其他部门对你的期望和需求,要合作。
能够理清楚这一点的,就已经很厉害了。
不要成为那种人:去外企面试,面试官问它药物管理职责。
它不屑的说,数药片、看试剂瓶,有啥好数的。
对对对,你说的都对,面试官面无表情请它走人。
平庸的人眼里,啥都很简单。
如果你面试外企,期望具备系统整合的知识体系、掌握复杂的技能,幻想免费就能搜索到是不切实际的(你搜呗),每位加入的会籍成员都说找了无数资料,无语得很。
是时间停止浪费时间精力,看着别人不断增值而你在贬值了。欢迎加入会籍。
临床试验实施过程中非常重要的一个环节,在于确保受试者接受标准治疗。不同于中医药的因人而异,化药需要按体重系数(例如,肿瘤药物)或等量给予药物,不能有差异,遇到AE后及时调整用药,不能服用禁忌药物。
长久以来,数量不菲的药厂和临床试验从业团体对药物管理职责存在严重认知错误,认为试验药物IMP仅允许用于临床试验受试者的要求,就是确保药物的存储、发放和回收全程可追溯。
实际上,临床试验规划和管理、监查过程,Drug Accountability是一项重要职责。
处方怎么开具?特殊处方怎么处理?怎样提前一晚上开处方,但当时并不知道第二天会随机出什么药物编号,怎么办?而且方案要求,第二天受试者前来site才能IWRS,怎么办?
片剂,应该设计什么包装?如何清点?怎样提醒受试者服用?是餐前餐后还是固定时间点?受试者外出旅游,能不能用小药盒自行分装?
包装盒为什么需要携带回来?如果跨国转运,这些病史采集、药物发放遭遇Site不一,编号问题,受试者未在IWRS录入等怎样快速解决?
药物为冻干粉针时,怎样冻融复苏,配液,并完成输注?如果盲态,怎么处理?
哪些药物,为什么在方案中会规定有用药依从性?怎么评价用药依从性并处理?直接劝退这种简单粗暴没文化的方式吗?
国内机构和申办方,不少还停留在强调药物领药人必须是受试者,必须是护士,必须是Sub-I这些奇葩看法,完全没有将视野放在许多重要环节,确保数据有效。
药物怎样设计标签,怎么设计提醒卡,让受试者能轻松的按照提示在家里服用药物?毕竟,没有谁会记得在医院接受随访时那些话语,写在纸上会好很多。如何设计?如何上报伦理备案?如何给受试者?这就是涉及运营管理的问题,毕竟高效经济的方式,才有现实可操作性,不然CRC和CRA忙不过来,就帮不上帮反而成为PD。
……略,会员登录网站查看
CRA登录网站查看:【中心监查】系列八十四||药物管理职责Drug Accountability
请登录网站查看,例如:


其中,CRA十二讲幻灯视频,会员登录可见。
本周六加入会籍,还可赠送《中心管理手册》和《监查工作指引》
欢迎垂询。
如果是企业,就得学习如何制作一系列表格:
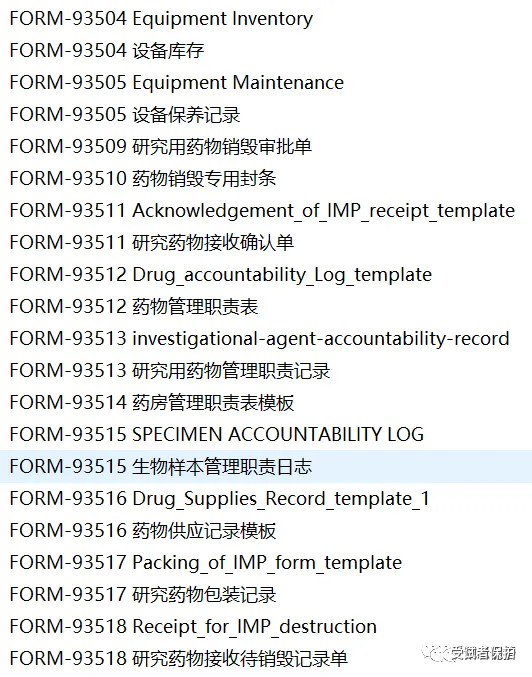
企业可联络,获取SOP和文档支持服务,直接获取文档设计服务。
欢迎个人加入CTBMI俱乐部会员,输入“会籍”、“付费”可获知详情。